Der Lichen planus gehört nicht nur der Dermatologie
Der Lichen planus ist eine komplexe, immunvermittelte Erkrankung mit vielfältigen kutanen und mukosalen Manifestationen. Neue Erkenntnisse zur Pathogenese und Systematik schärfen das Verständnis. Entscheidend sind vor allem zwei Dinge.
Heutzutage wird der Lichen planus nicht mehr ausschließlich als dermatologische Erkrankung wahrgenommen. Auch Gastroenterologen, HNO-Ärzte, Gynäkologen, Proktologen und Augenärzte sind gefordert. Im Konzert der entzündlichen Dermatosen rangiert diese hautlastige Autoimmunerkrankung hinter den Ekzemen aller Arten, der Psoriasis und der atopischen Dermatitis auf Platz vier der Aufmerksamkeitsskala. Wir Dermatologen lieben unsere „Knötchenflechte“.
Die fast schon lyrischen Beschreibungen der etwa 0,1 bis 0,2 cm großen Effloreszenzen zeugen von dem Respekt, den wir unserer „Serenissima“ entgegenbringen. Klinisch eindrucksvoll und eigenwillig im Verlauf präsentieren sich die rot-lividen, festen, oberflächenglatten, plateauartig erhabenen Papeln dem Kundigen in leichter diagnostischer Zugänglichkeit.
Oftmals weisen sie einen eigentümlich lackartigen Glanz auf, als wären sie für den Betrachter frisch poliert worden.
Wenn der prüfende Blick dazu noch das Charakteristikum der „Lichenknötchen“ entdeckt, die linearen, weißlichen Wickham'schen Musterungen, die sich klinisch und unter dem Auflichtmikroskop bei wenigen Tropfen eines Immersionsöls besonders gut präsentieren (ein phonetischer Tipp: Louis-Frédéric Wickham war Franzose), dann steht die Diagnose felsenfest ohne Wenn und Aber – ein Zeugnis hoher dermatologischer Diagnosekunst.
Durch die Konfluenz mehrerer Papeln können sich großflächige Plaques bilden. Eine Schuppung ist beim Lichen planus eher die Ausnahme (histologisch: orthokeratotische Verhornung). Dagegen gehört ein milderer Juckreiz zu seinen vergleichsweise inkonstant auftretenden Symptomen.
Symptomatik und Pathophysiologie
Während Patienten mit atopischer Dermatitis ihren quälenden neurogenen Juckreiz intensiv mit den Fingernägeln bearbeiten, bleibt dieser Reflex beim Lichen planus aus. Man findet keine Kratzexkoriationen. Die Isomorphie der Läsionen, am besten erkennbar an den linear angeordneten Formationen (Köbner-Phänomen), ist ein weiteres Kennzeichen des eruptiv-aktiven Lichen planus:
Diese scheinbar banalen Strukturbesonderheiten haben einen hohen erkenntnistheoretischen Wert, denn wie so oft liegt das Geheimnis des Realen nicht im unmittelbar Sichtbaren, sondern in den verborgenen pathophysiologischen Mechanismen, die das Sichtbare hervorbringen. Diesem Satz liegen die Grundprinzipien der klinischen Medizin zugrunde. Man könnte ihn als ihren „kategorischen Imperativ“ bezeichnen, aber dazu später.
Beim Lichen planus (LP), ob kutan, oral, ösophageal oder genital, findet sich der Schlüssel zur Pathogenese in der triggerbaren Hyperreagibilität der Epithelzelle. Präziser ausgedrückt: in dem vielseitig aktivierbaren immunologischen Feuerwerk der keratinogenen (Fähigkeit zur Hornbildung) Plattenepithelien von Haut und hautnahen Schleimhäuten.
Wie durch das scheinbar so „einfache“ Köbner-Phänomen belegbar, ist die mit einer LP-Imprimatur versehene Epithelzelle befähigt, einen höchst banalen mechanischen Reiz (zum Beispiel eine einfache Kratzspur) in eine spezifische Entzündung („Lichen-planus-Effloreszenz“) umzusetzen. Das nicht aktivierte, physiologische keratinogene Plattenepithel hingegen würde einen banalen mechanischen Reiz völlig ignorieren, einen mechanischen Dauerreiz stereotyp höchstens mit einer einfachen Schwiele beantworten.
Ätiologie und Forschungsbedarf
Was die Ätiologie und Pathogenese des Lichen planus betrifft, so dürfen wir in den nächsten Jahren auf neue molekulare Erkenntnisse, zum Beispiel hinsichtlich des veränderten Transkriptoms des LP-Keratinozyten hoffen. Denn genau genommen hat sich seit der Erstbeschreibung durch den großen englischen Dermatologen Erasmus Wilson im Jahr 1869 nichts Grundlegendes getan.
Ja, über das losgetretene inflammatorische Zytokinspektrum wissen wir einiges. Aber eine grundlegende Idee zur Pathogenese? Fehlanzeige. Diese leicht resignative Aussage betrifft allerdings nicht nur den Lichen planus, sondern auch etwa 3000 weitere dermatologische Diagnosen. Immerhin haben wir Hautärzte inzwischen verinnerlicht, dass der Lichen planus keine rein dermatologische Affäre ist.
Dieses Skript ist ein Gemeinschaftswerk: Wolfgang Kreisel, emeritierter Gastroenterologe aus Freiburg, und ich haben uns auf den Weg gemacht, die nichtkutanen Manifestationen des Lichen planus näher zu beleuchten, um das Prinzip dieser polytopen „Systemerkrankung“ besser verstehen zu können.
Wir wollen, und das ist vorrangig an die „erstdiagnostizierenden Kollegen“ gerichtet, bei dieser Autoimmunerkrankung für einen multidisziplinären Ansatz werben.
In eigener Sache. Die DMEA – Connecting Digital Health ist Europas wichtigstes Event für Gesundheits-IT. Es findet vom 21. bis 23. April auf dem Berliner Messegelände statt. Schauen Sie vorbei und lernen Sie dort das Software-Unternehmen Ingrano Solutions kennen, mit dem Altmeyers Enzyklopädie zusammenarbeitet. Die IT-Spezialisten werden ihr Pionierprojekt Patienteninfo 360° vorstellen, einen neuen Service für Patientenkommunikation. Sie finden Ingrano Solutions auf dem Stand der ID Berlin (Halle 4.2, Nummer A-105) und auf dem eigenen Unternehmensstand (Halle 3.2, Nummer D-103). Schreiben Sie uns, falls Sie Rückfragen haben.
Bei der Diskussion über die Pathogenese dieser Erkrankung kam plötzlich die scheinbar banale Frage auf, ob es sich bei dem Lichen planus um eine Systemerkrankung im klassischen Sinne handelt. Hierzu aus Freiburg und Bochum ein klares „Jein“.
Definiert man „Systemerkrankung“ (zum Beispiel die Psoriasis) als Multiorganerkrankung, die sich gleichzeitig oder auch sukzessiv in mehreren Gewebetypen eines oder mehrerer Organe manifestiert, dann schließt diese Definition den Lichen planus als Systemerkrankung aus.
Fokus aufs keratinogene Plattenepithel
Der Lichen planus kann sich zwar ebenfalls multiorganisch ausbreiten, jedoch ist nur ein einziger Gewebetypus beteiligt – das keratinogene Plattenepithel. Dies begreifen wir als immunologische und funktionelle Einheit.
- Leitsatz: Der Lichen planus kann sich zwar multiorganisch „ausbreiten“, ist aber ausschließlich auf das keratinogene Plattenepithel fokussiert. Er erfüllt somit nicht die Definition einer Systemerkrankung.
Das Prinzip der plattenepithelialen Funktionseinheit umschreibt ein funktionell, embryologisch und immunologisch zusammenhängendes keratinozytäres System, das durch die Mannigfaltigkeit seiner Organmanifestationen (Haut, oberflächennahe Schleimhäute, Kornea) imponiert. Es basiert auf der in allen Organen vergleichbar strukturierten Grenzregion zwischen außen und innen, der wichtige Kernaufgaben (Barrierefunktion, hohe immunologische Kompetenz) zukommen.
Organsysteme wie Darm, Harnblase oder Gefäße verfügen über eine nicht-keratinogene und damit andersartig strukturierte Auskleidung ihrer Oberflächen. Diese sind aufgrund ihrer immunphänotypischen Merkmale nicht in der Lage, die spezifische (histologisch als Interface-Dermatitis/Mukositis bezeichnete) lichenoide Entzündung des Lichen planus zu erzeugen.Dazu ist ausschließlich das keratinogene Plattenepithel befähigt.
Folgt man diesem Postulat, so wird das Verteilungsmuster des LPs verständlich. Betroffen sind ausschließlich die Haut und die hautnahen Schleimhäute (nicht-verhornendes keratinogenes Plattenpithel), wie Mund und Nasenvorhof (die respiratorische Nasenschleimhaut ist nicht beteiligt), Ösophagus (nicht jedoch die Schleimhaut des Magens), Vulva und Vagina, Penis mit Fossa navicularis urethrae (nicht jedoch die mittlere und obere Urethra) sowie, kaum bekannt, die Cornea oculi (nicht jedoch die Konjunktiven).
Kornea gehört ins Reich der Plattenepithelien, die Konjunktiva nicht
Der LP-Befall der Kornea mag in dieser konzeptionellen Übersicht zunächst belanglos erscheinen. Das ist er aber nicht. Diese klinische Beobachtung verdeutlicht sogar das Prinzip des „plattenepithelialen Kontinuums des Lichen planus“.
Die Lösung: Die Kornea gehört ins Reich der Plattenepithelien, die Konjunktiva hingegen nicht, denn diese ist im Gegensatz zur Kornea nicht von einem keratinogenen Plattenepithel überzogen, sondern von einem mehrschichtigen, kubischen bis prismatischen Epithel mit zahlreichen schleimproduzierenden Becherzellen.
Dieser Epitheltypus gehört funktionell und vor allem immunologisch nicht zur plattenepithelialen kutan-mukosalen Achse. Er spielt dementsprechend immunologisch in einer anderen Liga. Die Expression einer spezifischen, lichenoiden Interface-„Mukositis“ ist für diesen Epitheltypus per se ausgeschlossen.
Folgt man diesen Maximen, so ergibt sich nachfolgend gelistete (nur scheinbar komplexe) klinische Übersicht:
Übersicht der unterschiedlichen klinischen Phänotypen des Lichen ruber
Klassischer kutangeprägter Lichen planus:
- Lokalisierter (gewöhnlicher) Lichen planus der Haut und angrenzende Schleimhäute
- Generalisierter (exanthematischer) Lichen ruber der Haut und angrenzende Schleimhäute
- Erythrodermischer (universeller) Lichen planus der Haut und angrenzende Schleimhäute (seltene Maximalvariante)
Phänotypische Varianten des klassischen kutanen Lichen ruber:
- Blaschkoider Lichen planus (Lichen planus striatus/Kutane Mosaikdermatose)
- Zosteriformer Lichen planus (Isotopische Antwort in einer durch eine frühere Zosterinfektion immunologisch veränderten Hautregion)
- Anulärer Lichen planus (kleinherdige Ringstrukturen)
- Verruköser Lichen planus (vorwiegend an den Streckseiten der Unterschenkel)
- Atropher Lichen planus (als Abheilungsphase mit ausgedünnter Epidermis, meist gräulich pigmentiert – klinische Nähe zur „Ashy dermatosis“)
- Lichen planus pigmentosus (häufig inverse Topographie, ausgeprägte Pigmentinkontinenz)
- Bullöser Lichen ruber (basierend auf einer exsudativen Interface-Dermatitis)
- Aktinischer Lichen ruber (vor allem in entwickelten Zonen, UV-belichtete Hautareale, ungewöhnliches Alter/Kinder und junge Erwachsene)
Organbezogene (monotopische oder polytopische) Lichen-planus-Varianten:
- Oraler Lichen planus (syn. Lichen planus mucosae: Plaqueförmig, flächig erosiv, mögliche Beteiligung des Nasenvorhofs)
- Ösophagealer Lichen planus (OLP/Lichen-planus-Ösophagitis):
- Anogenitaler Lichen planus: 1) Vulvovaginaler Lichen planus 2) Analer Lichen planus
- Adnexieller Lichen ruber (Hautadnexe): 1) Follikulärer Lichen ruber (follikulärer Knötchen, Follikelatrophie, Verlust des Immunprivilegs der Stammzellnische des Follikels mit konsekutiver narbiger Alopezie, Graham-Little-Syndrom) 2) Lichen planus der Nägel mit Atrophie oder vollständiger Verlust der Nagelplatte (Verlust des Immunprivilegs der Stammzellnische des Nagelwurzelepithels)
- Lichen planus palmoplantaris (schwielenartige Entzündungen an Druckstellen)
- Okulärer Lichen planus (betroffen ist die mit nichtverhornendem Plattenepithel versehene Kornea, nicht die Konjunktiven)
Nach diesen Ausführungen haben wir uns hinsichtlich der Ätiologie dieser etwas geheimnisvoll daherkommenden, interdisziplinären, autoimmunologischen LP-Erkrankung auf eine gängige Definition geeinigt. Diese lautet:
Der Lichen ruber (LP) ist eine erworbene, nicht-systemische, polyätiologische, mono-häufig multiorganisch angelegte, T-zellvermittelte (autoimmunologische) Interface-Dermatitis/Mukositis des mehrschichtigen, keratinogenen Plattenepithels.
Über induzierende virale Infekte (auffällig häufig sind Assoziationen mit SARS-CoV-2-Infektionen) wurde mehrfach berichtet. Die Induktion durch allerlei Medikamente und Vakzine (SARS-CoV-2) ist gut belegt, ebenso die mechanische Triggerung (Kratzen, Reiben, flächiger Druck beim Lichen palmo-plantaris etc.).
Der zusätzliche Blick auf die Medikamentenpalette lohnt sich, da ein breites Sortiment in Verdacht steht: zum Beispiel NSAR, Betablocker, Chloroquin, ACE-Hemmer, Interferon und Checkpoint-Inhibitoren. Beim oralen LP können auch lokal irritierende Substanzen wie Amalgam, Quecksilber oder Gold, selbst mechanische Irritationen an den Zahnkontaktstellen einen Lichen planus oder eine Lichen-planus-artige lichenoide Mukositis induzieren.
Therapeutisch ist hierbei ein Wechsel der Kontaktmaterialien anzuraten. Die Assoziation zwischen LP und verschiedenen Autoimmunerkrankungen wie primär biliärer Cholangitis, Autoimmunthyreoiditis, Myasthenia gravis, Alopecia areata, Vitiligo, Thymom und autoimmuner Polyendokrinopathie ist ebenfalls zur Genüge belegt. Dabei ist nicht immer klar, was Henne und was Ei ist.
Komorbidität „Diabetes mellitus“!
Eine Assoziation von Lichen planus und Diabetes mellitus kommt häufig vor. Bei jedem zweiten LP-Patienten besteht eine Störung des Glukose-Stoffwechsels und bei jedem vierten ein manifester Diabetes mellitus. Für die Trilogie aus oralem LP, Diabetes mellitus und Hypertonus wurde sogar ein Syndrom geschaffen, das „Grinspan-Syndrom“.
Die Pathogenese des LP ist bisher lückenhaft geblieben. Einmal in Gang gebracht, entfaltet der LP ein ein autochthon perpetuierendes Entzündungspotenzial mit einem unterschiedlich langen Kontinuum. Es kann davon ausgegangen werden, dass eine Autoimmunreaktion gegen Epitope basaler keratinogener Plattenepithelien vorliegt. Die induzierte apoptotische Reduktion der basalen Keratinozyten kann als gemeinsame Endstrecke der Lichen-planus-Reaktion aufgefasst werden.
In diesem Zusammenhang ist auch die Hochregulierung von BIRC5 beim LP interessant, ein Gen, das für „Survivin“ kodiert. Dies ist ein multifunktionales Zytokin, das eine janusartige Rolle spielt: einerseits bei der Hochregulierung der Zellproliferation, andererseits bei der Verhinderung der Apoptose.
Für die klinische Prognose des „Schleimhautlichen“ ist dies insofern bemerkenswert, als Survivin auch in den LP-induzierten mukosalen Präkanzerosen und Plattenepithelkarzinomen hochreguliert ist. Dieser Befund könnte eine Erklärung für die onkogene Potenz des mukosalen Lichen planus liefern.
Nun zu den topographisch verwandten Phänotypen des oralen und des ösophagealen Lichen planus:
Der orale Lichen planus (OLP) wird bei erstaunlichen 75 Prozent (!) der Patienten (w:m=3:1) mit integumentalem Befallsmuster beobachtet und ist die häufigste Schleimhautmanifestation des LP. Sein Verlauf ist eminent chronisch. Typisch sind, wie auch in der Haut, symmetrische, netzartige oder nummuläre weiße Plaques; auch disseminierte, 0,1 cm große weiße Papeln an Wange und/oder Zunge und/oder Gingiva.
Lichen planus der Mundschleimhaut
Eine komplikative Besonderheit stellt der schmerzhafte und therapieresistente, erosive Lichen planus der Mundschleimhaut dar, der einer permanenten Lokal- und/oder Systemtherapie bedarf. Bei diesem aggressiven Phänotypus konnten in läsionaler Schleimhaut in einem hohen Prozentsatz HCV-RNA und TTV-DNA (transfusion-transmitted-virus) nachgewiesen werden.
Klinisch bedeutsam ist, dass beim oralen LP als einer potenziell malignen oralen Erkrankung (OPMD) mit Transformationsraten zwischen 0,44 bis 2,28 Prozent gerechnet werden muss.
Der ösophageale Lichen planus tritt bei bis zu 50 Prozent (!) der Patienten mit kutanem oder oralem LP auf. Dieses Befallsmuster ist bisher an den klassischen dermatologischen Lehrbüchern spurlos vorbeigegangen. Bei 70 bis 80 Prozent dieses Klientels handelt es sich um ältere (Erstvorstellungen im siebten Lebensjahrzehnt) Frauen. Der ösophageale Lichen planus verläuft häufig asymptomatisch. Zeichen der Dysphagie können sich bemerkbar machen.
Zur klinischen Dynamik: Der Befall von Haut und Ösophagus erfolgt häufig nicht gleichzeitig, sondern zeitversetzt. Intervalle von Jahren bis Jahrzehnten sind möglich. Der Schleimhautbefall ist deutlich hartnäckiger als der Hautbefall.
Endoskopisch zeigen sich bei diesem Phänotyp nicht selten Schleimhautablösungen und -einrisse, Trachealisierung (heißt: Endoskopisch sieht man Ringstrukturen im Ösophagus wie bei der Trachea) und Hyperkeratosen.
Diagnostik und Therapie
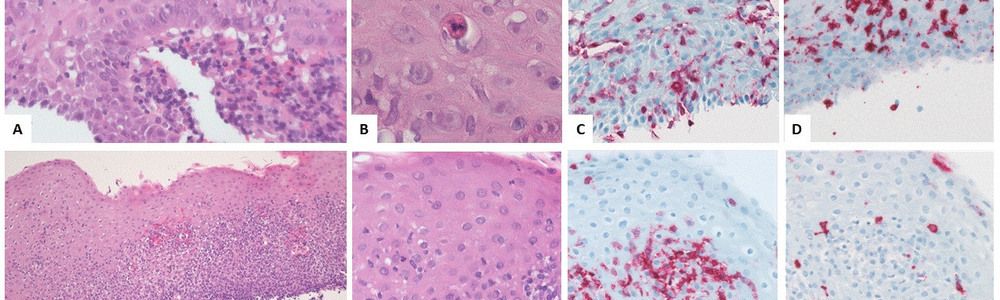
Bei chronischem Verlauf kann es zu einer vernarbenden Ösophagusstenose kommen. Die Histologie entspricht pathogenetisch einer lichenoiden Interface-Mukositis mit T-lymphozytären Infiltrationen des Oberflächenepithels, Epithelzellapoptosen (Civatte-Körperchen), Dyskeratose und Hyperkeratose. Sie sollte zur diagnostischen Absicherung erfolgen.
Immunhistologisch finden sich, wie auch beim kutanen LP, Fibrinogenablagerungen entlang der Basalmembranzone. Mit anderen Worten: Das feingewebliche Bild des ösophagealen LP ist dem des kutanen LP vergleichbar. Dies war nach unseren Vorbetrachtungen erwartbar.
Auch der ösophageale Lichen ruber (ELP) muss als Präkanzerose bewertet werden. In verschiedenen Studien werden Ösophaguskarzinomraten von 4,5 Prozent, bei dysphagischen ELP-Patienten bis zu 10 Prozent berichtet. Diese Zahlen sollten jedem Arzt zu denken geben.
Therapie: In diesem Skript ist diese nur kursorisch aufgeführt. Aufgrund der multiorganischen Manifestationen erfordert der LP einen multidisziplinären Ansatz unter Einbeziehung von Dermatologen, Zahnärzten, Gynäkologen, Gastroenterologen und Histopathologen.
Topische Kortikosteroide sind die Behandlung der ersten Wahl. In therapieresistenten Fällen kommen Tacrolimus, Methotrexat (MTX), Apremilast oder systemische Kortikosteroide in Betracht. Die europäischen Leitlinien zur LP-Therapie wurden kürzlich veröffentlicht und können dort nachgelesen werden.
Regelmäßige Nachsorge unerlässlich
Unsere Ausführungen machen deutlich, dass der Lichen planus der Haut und der Mundschleimhaut in der DNA der Dermatologen bestens verankert ist. Das wird schon an der Vielzahl der gut dokumentierten Varianten mit ihren topografischen Besonderheiten ersichtlich. Der ösophageale Lichen planus hingegen, der interessanterweise erst im Jahr 1982 beschrieben wurde, wird deutlich unterdiagnostiziert.
Das liegt zum einen daran, dass ein erheblicher Teil der LP-Patienten klinisch keine ösophagealen Symptome aufweist. Zum anderen daran, dass den primär diagnostizierenden und behandelnden Ärzten diese Manifestation überhaupt nicht bekannt ist. Umso mehr sind alle bestrebt, eine interdisziplinäre Früherkennung zu veranlassen.
Beim kutanen Lichen planus gibt es im Gegensatz zu allen Varianten des mukosalen LP kein erhöhtes Karzinomrisiko. Der mukosale LP von Vulva/Vagina, Mund und Ösophagus muss jedoch als Präkanzerose bewertet werden, mit einem relevanten Risiko zur malignen Progression, das mit 2 bis 10 Prozent veranschlagt werden muss. Auch bei negativer Befundung ist eine regelmäßige Nachsorge unerlässlich. (Autoren: Peter Altmeyer und Wolfgang Kreisel)
